摘要:2025 年伐美妥司他价格依旧高昂,日本原研 200mg*112 粒装约 1373 美元且需自费。该药已在超 30 国上市,中国内地仍处临床三期,预计 2026 年获批,海南先行区可特许使用。用药前需完善检查、调整合并用药,提前预防不良反应并制定随访计划 。
在血液肿瘤治疗领域,伐美妥司他凭借其针对复发或难治性成人 T 细胞白血病 / 淋巴瘤(ATLL)和外周 T 细胞淋巴瘤(PTCL)的显著疗效,成为众多患者关注的焦点。药物价格、全球上市进展及用药规范,是患者制定治疗决策的关键因素。以下将为您详细解读 2025 年伐美妥司他的最新动态。
一、2025 年伐美妥司他最新价格
伐美妥司他作为创新药物,2025 年市场定价仍处于较高水平,且价格存在一定波动。
(一)原研药定价
日本原研的伐美妥司他,规格为 200mg*112 粒,目前市场价格约 1373 美元(按当前汇率换算,约合人民币 9700 元) ,由于尚未纳入医保,需患者完全自费,对许多家庭而言是不小的经济负担。
(二)购买渠道价格差异
不同购买渠道价格存在差异。医院药房的售价相对固定,而通过跨境购药,除药价外,可能还需支付服务费。部分国际药房推出会员优惠政策,患者可关注相关信息,以获取更实惠的购药价格。需特别注意,药品价格受汇率波动、供应链变化影响明显,建议通过正规医院、官方授权药房等渠道获取实时报价。
二、伐美妥司他全球上市情况
伐美妥司他的全球上市进程逐步推进,但各国审批进度有所不同。
(一)已批准地区
2022 年 9 月 26 日,日本率先批准伐美妥司他上市;随后在 2023 - 2024 年间,美国食品药品监督管理局(FDA)和欧盟药品管理局(EMA)也相继通过审批。截至目前,该药物已在全球 30 多个国家上市销售,为更多患者带来治疗希望。
(二)中国市场状态
遗憾的是,伐美妥司他尚未获得中国国家药品监督管理局(NMPA)批准,目前处于临床三期试验阶段。不过,在海南博鳌乐城国际医疗旅游先行区,符合条件的患者可申请特许使用。患者需准备完整病历资料,通过正规流程申请,以获取用药机会。
(三)上市时间预测
根据药品审评流程和进度,预计伐美妥司他最快于 2026 年在中国内地获批上市。值得关注的是,部分国内药企已启动仿制药研发工作,未来有望为患者提供更多选择。患者可通过国家药品监督管理局官网,定期查询最新审批动态;也可咨询指定医疗机构,详细了解特许用药政策及申请流程。
三、伐美妥司他用药准备
规范使用伐美妥司他,治疗前的充分准备至关重要。
(一)必要检查项目
用药前,患者需完成血常规、肝功能、心电图等基础检查,以评估身体基本状况。对于特定患者,还需进行基因检测,确认药物靶点表达情况,确保用药精准有效。
(二)合并用药调整
正在服用强效 CYP3A4 抑制剂的患者,需在用药前至少停用 1 周;使用抗凝药物的患者,需在医生指导下调整剂量,避免药物相互作用,降低用药风险。
(三)不良反应预防
为应对可能出现的不良反应,建议患者预先准备止吐药物和抗过敏药物。治疗初期,部分患者可能出现乏力症状,此时应避免驾驶机动车或操作精密仪器,确保自身安全。
(四)随访计划制定
患者需建立规律的复诊时间表。治疗前 3 个月,建议每 2 周复查血常规,密切监测血液指标变化;3 个月后,可每月监测一次。一旦出现异常指标,应及时就医,由医生调整治疗方案。
规范的治疗前评估和准备是保障用药安全、提升治疗效果的关键。患者务必严格遵循医嘱,做好各项准备工作,积极配合治疗,以获得更好的治疗结果。
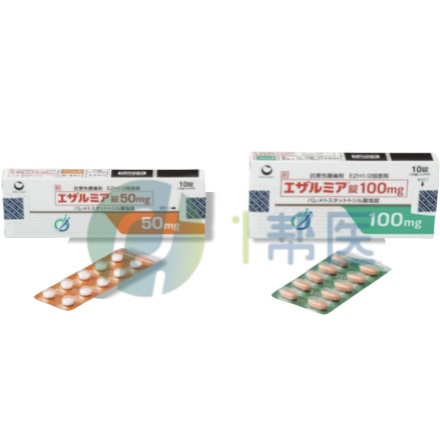
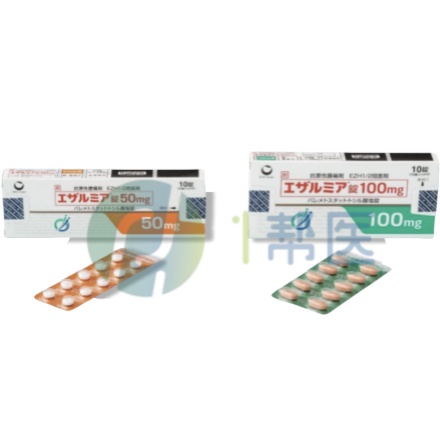
 伐美妥司他(Valemetostat)
伐美妥司他(Valemetostat) 片剂
50mg*10片|100mg*10片
 日本第一三共
日本第一三共
首款EZH1/2双重抑制剂,治疗白血病、淋巴瘤有效率48%
2025-04-29 13:11:51
2025-04-29 13:00:18
2025-04-29 12:48:34
2025-04-29 12:31:26
2026-03-17 22:26:02
2026-03-17 22:06:52
2026-01-15 13:55:13
2026-01-15 13:47:42
2026-01-15 11:56:27
2026-01-15 11:40:40